プラスとマイナスの電気を帯びた「イオン」だけからなる物質を「塩」と呼びます。
プラスとマイナスがお互いに強く引き付け合うために、室温で塩はイオンが規則正しく配列した固体の結晶となります。身近な「塩」の代表が『食塩』です。
水を加えないで食塩を液体にするには801℃まで加熱しなければなりません。氷が解けて水になる温度は0℃ですが、塩が溶ける温度は極めて高温であると考えられていました。
ところが、15~20年ほど前に室温で液体状態の新しい「塩」が合成されました。
これが『イオン液体』です。
人類が初めて手にした『イオン液体』は、極めて不思議な性質を持っていました。
イオン液体は室温付近ではほとんど蒸発しません。コップに入れて放置しても水のように無くなりはしないのです。
またガス化もしにくく、燃えません。電気をよく伝え、いろいろな物質を溶かすことができます。広い温度範囲で液体のままです。
イオン液体の性質をまとめてみますと・・・・
- イオンだけで構成され、大気中で取り扱いが可能(安定している)
- 高いイオン伝導性を有する(導電性がある)
- 電気圧が極めて小さい不揮発性の液体(極めて蒸発し難い)
- 不燃、もしくは難燃性の液体で、高い熱分解温度を有する(約400℃の範囲)
- 電気分解されにくい(耐電圧が高い)
- 化学的安定性と物質の溶解力が高い(何でも溶かす)
- 高い比熱を有し、熱伝導体としても使用できる
私たちの研究グループは、肥料や洗剤などに使われるアンモニアと呼ばれる分子を特別な構造に加工すると『イオン液体』になることを発見しました。合成されたイオン液体は、ガムシロップの様に少しとろみのある透明淡黄色の液体でした。
調べてみると-90℃から約330℃の範囲で液体となり、電気も良く伝え、高い耐電圧を持っていることが判りました。マッチで火をつけても燃えません。そこでこのイオン液体を電池に応用しようと考えました。
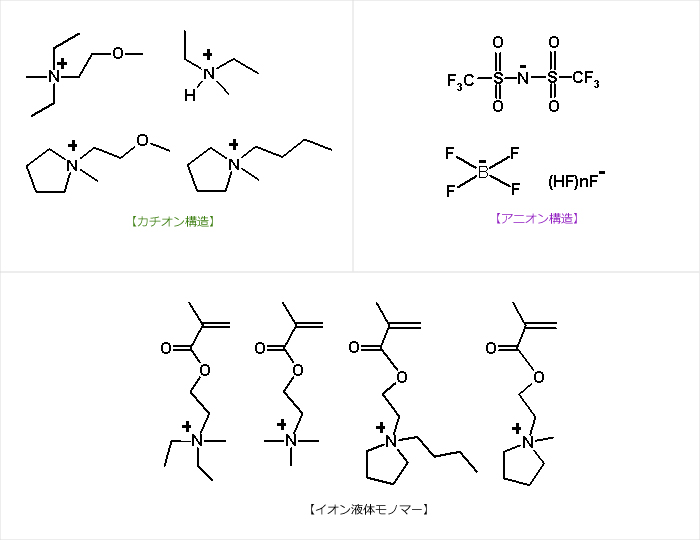
今までに当研究室の学生が合成したイオン液体の分子構造を示します。
カチオン分子内に反応性の二重結合を持った、重合性イオン液体(イオン液体モノマー)も合成することが出来ました。このイオン液体モノマーからは、イオン液体の性質を持ったプラスチックが得られると期待されています。
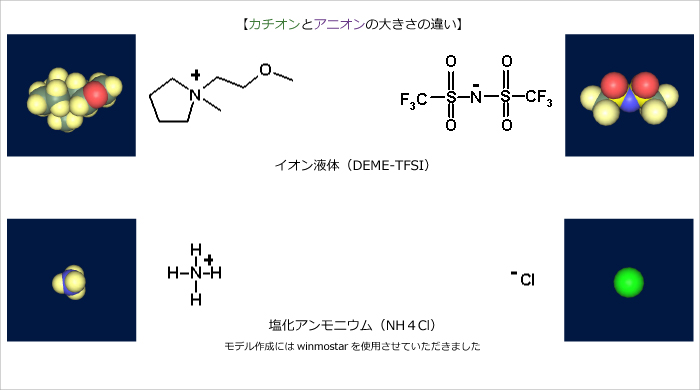
イオン液体は、カチオンとアニオンのみから構成される塩ですが、皆さんが知っている塩化アンモニウム(NH4Cl)も、+NH4のカチオンとCl―-のアニオンのみからなる物質です。しかし塩化アンモニウムは、室温では食塩と同じように固体の粉末です。どのようにしたらイオン液体を作ることが出来るのでしょうか?
手っ取り早い方法は、カチオンとアニオンの大きさを嵩高くすることです。研究室で合成したDEME-TFSIというイオン液体と塩化アンモニウムの分子構造をモデルで比較してみましょう。
DEME-TFSIは塩化アンモニウムに比べて分子のサイズが極めて大きいことが一目瞭然です。
嵩高いアニオンとカチオンを組み合わせるとイオン液体になりやすくなります。
当研究室では、新しいイオン液体の合成とその物理化学特性評価と、イオン液体の新しい利用方法の探索研究を行っています。